近些年来,聊到免疫疗法,必然会说到的就是PD-(L)1抑制剂和CAR-T细胞疗法——前者是因为其在多种实体肿瘤适用中的普适性和有效性,即可以在任何类型的肿瘤中适用,同时可以发挥出不错的治疗性效果;后者则是因为其在血液肿瘤中的出彩表现,即使是晚期多次复发的血液肿瘤患者,也可以获↙得超过80%的缓解率。
也是因为如此,如今免疫治疗中最为火热的便是CAR-T细胞疗法和PD-(L)1抑制▼剂疗法。但是PD-(L)1抑制剂疗法一直为人诟病的便是无法达到更高的有效率,而CAR-T细胞疗法则一直在不断寻求实体肿瘤治疗的突破——毕竟血液肿瘤患者相比于实体肿瘤患者而言,实在是太少。而只有打破这道壁垒,CAR-T细胞疗法才能发挥更好的治疗效果。
在前面的文章中我们也提到过,免疫疗法最大的优∞点之一就是兼容性,不仅是免疫疗法可以和其他疗法比如放化疗和靶向药联合使用,不同的免疫疗法之间也可以互相结合来提高治疗效果,那么如果CAR-T细胞疗法联合PD-(L)1抑制剂疗法呢?
一方面,CAR-T细胞具↑有高效杀伤异质性肿瘤细胞且避免对正常细胞毒副作用的特性,而PD1抗体能消除肿瘤微环境(TME)对回输的CAR-T细胞活性的抑▆制,且能原位激活肿瘤浸润特异性T细胞的功能,避免全身用药可能产生的毒副作用。
另一方面,通过CAR-T细胞的肿瘤趋向性,CAR-T细胞通过血液循环后重新分布,聚集在肿瘤部位,在肿瘤局部高水平表达PD-1抗体,将同时克服CAR-T细胞治疗与免疫检查点抗体治疗各自的缺陷,发挥两者的协同效应,提高疗效,同时降低治疗成本。
而正是因为这种想法,最终呈现在我们眼前的就是白泽T技术,同时该项研究的成果也在今年ASCO上进行了发表。
此次的白泽T技术,更具体的来说是aPD1-MSLN-CAR-T细胞治疗技术,属于复合免疫疗法,结合了CAR T细胞和PD-1抗体的优点,对于实体瘤具有独特的治疗优势。
间皮素(Mesothelin, MSLN, meso)为表达在肿瘤细胞表面的蛋白。靶向识别MSLN的CAR-T细胞是肿瘤治疗领域的新星。aPD1-MSLN-CAR-T细胞通过非病毒载体PiggyBac转座子系统在体外修饰外周血单个核细胞(PBMC),使其能特异性识别肿瘤细胞上表达的MSLN,同时能自分泌PD-1抗体。可以说这项新的技术是当今2项最顶尖的免》疫细胞疗法的集合体。
那么它是否可以对抗晚期实体肿瘤呢?
这项一期临床试验于2018年8月开始,入组的患者为多线标准治疗失败的MSLN阳性的复发/难治性实体瘤患者,于2019年12月给最后一例患者回输最后一次细胞。入组患者的平均年龄为54.5岁(范围39-67岁),2例患者为男性,8例患者为』女性——注意这里并没有限制入组患者的肿瘤种类。
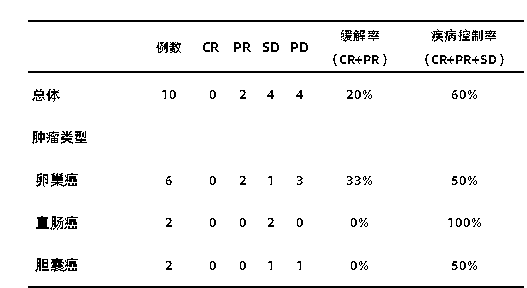
CAR T细胞的第一剂量组为5×10^6/kg,第二剂量组为5×10^7/kg和第三剂@量组为1×10^8/kg,每个剂量组每个疗程回输一次细胞,共回输至少2个疗程。每28天进行疗效评价和安全性评价,记录不良@ 事件(AE)发生情况
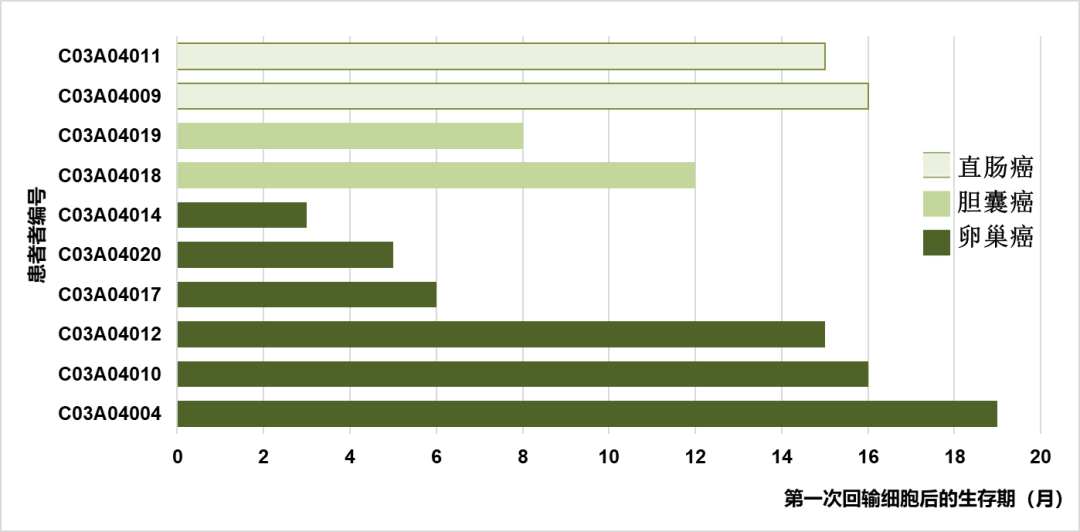
截至2020年4月患者第一次回输细胞后的生存期(月)
本文章收录于ASCO会议海报区。第一作者为上海市第十人民医院方珏敏博士,通讯作者为上海市第十人民医院许青教授。
许青 教授

同济大学附属上海市第十人民医院肿瘤科主任、肿瘤学教研室主任;
主任医师、教授、博士生导师;
同济大学癌症中心∏常务副主任;
上海市皮肤病医院肿瘤科主任;
第二军〓医大学海军系M.D.,第二军医大学内科学博士Ph.D.;
美国H.Lee.Moffitt癌症中心博士后、访问学者;
美国UC Davis癌症中心中美交流互访学者。
方珏敏 博士

同济大学医学院临床医学系博士;
同济大学附属上海市第十人民医院肿瘤科主治医师;
美国Mayo Clinic分子生物系访问学者。
